Model Atom Mekanika Kuantum
 Kajian Teoritik Terhadap Model Atom Helium Berdasarkan
Kajian Teoritik Terhadap Model Atom Helium Berdasarkan
Model/Teori Atom Mekanika Kuantum: Pengertian, Gambar, Kekurangan dan Kelebihannya
Mungkin kalian tidak percaya atom itu ada, karena memang tidak ada seorang pun yang pernah melihatnya dengan mata biasa, termasuk para ahli kimia. Sesuatu yang tidak dapat dilihat oleh mata belum tentu tidak ada, misalnya angin. Kita dapat merasakannya melalui hembusannya.
Para ahli menerima keberadaan atom walaupun belum pernah melihatnya dengan mata biasa. Berdasarkan kesimpulan yang diperoleh dari percobaan ataupun eksperimen, para ahli mengajukan teori tentang model atom, yaitu suatu gambar rekaan atom berdasarkan eksperimen ataupun kerja teoritis.
Model atom hanya suatu gambaran, karena para ahli tersebut tidak tahu pasti seperti apakah bentuk atom yang sebenarnya. Bisa jadi suatu saat nanti ditemukan suatu model atom terbaru yang dapat menggugurkan atau menyempurnakan teori atom yang sudah ada dan mungkin ada di antara kalianlah yang menjadi penemunya.
Apa itu Atom?
Teori tentang atom sudah ditemukan sejak 400 tahun Sebelum Masehi (SM), oleh ahli filsafat Yunani, yaitu Leukippos dan Demokritos yang mencari asal mula semua benda di alam semesta. Mereka menyatakan bahwa semua benda terdiri atas bagian-bagian yang sangat kecil dan tidak mungkin dibagi-bagi lagi yang dinamakan atom (a: tidak, tomos: dibagi).
Pada abad ke-5 SM di India telah ada pendapat yang menyatakan bahwa tiap unsur benda terdiri atas satu sampai lima atom. Abad ke-8, Jabir seorang ilmuwan muslim menyatakan bahwa materi dibentuk oleh partikel dasar bermuatan yang menyerupai petir dan partikel, yang tidak dapat dibagi-bagi.
Selanjutnya perkembangan atom setelah abad ke-19 mulai bermunculan, dari model atom Dalton, Thompson, Rutherford, Niels Bohr hingga mekanika kuantum (modern). Nah, pada kesempatan kali ini kita akan membahas model atom mekanika kuantum. Berikut ini penjelasannya.
Model Atom Mekanika Kuantum (Modern)
Pada tahun 1913, berdasarkan analisis spektrum atom dan teori kuantum yang dikemukakan oleh Max Plank, Niels Bohr mengajukan model atom hidrogen, yaitu atom yang hanya mengandung satu elektron. Menurut Bohr elektron beredar mengitari intinya pada tingkat-tingkat energi tertentu, bagaikan planet-planet mengitari matahari dan elektron dapat berpindah dari tingkat energi satu ke tingkat energi yang lain.
Model Atom Bohr mempunyai beberapa kelemahan:
□ Teori atom Bohr hanya dapat menerangkan spektrum atom yang saderhana, misal Hidrogen, dan tidak dapat menerangkan yang lebih rumit (nomor atom > 1)
□ Teori Bohr tidak dapat menjelaskan pengaruh medan magnet dalam atom hidrogen.
Oleh karena itu, tidak mungkin membayangkan elektron beredar mengitari inti menurut suatu orbit berbentuk lingkaran dengan jari- jari tertentu. Kekurangan model atom Bohr disempurnakan dengan model atom mekanika kuantum yang dikemukakan oleh Erwin Schrodinger pada tahun 1927, seorang ilmuan dari Austria.
Teori Atom Mekanika Kuantum didasarkan pada dualisme sifat elektron yaitu sebagai gelombang dan sebagai partikel.
■ Menurut de Broglie, cahaya dapat berperilaku sebagai materi dan berperilaku sebagai gelombang (dikenal dengan istilah dualisme gelombang partikel).
■ Menurut Heisenberg, tidak mungkin menentukan kecepatan dan posisi elektron secara bersamaan, tetapi yang dapat ditentukan hanyalah kebolehjadian menemukan elektron pada jarak tertentu dari inti.
Erwin Schrodinger mengajukan teori yang disebut teori atom mekanika kuantum ”Kedudukan elektron dalam atom tidak dapat ditentukan dengan pasti yang dapat ditentukan adalah kemungkinan menemukna elektron sebagai fungsi jarak dari inti atom”.
Daerah dangan kemungkinan terbesar ditemukan elektron disebut orbital. Orbital digambarkan berupa awan, yang tebal tipisnya menyatakan besar kecilnya kemungkinan ditemukan elektron di daerah tersebut.
Elektron bergerak mengelilingi inti pada orbital. Orbital menggambarkan daerah kebolehjadian ditemukannya elektron. |
Kemudian Werner Heisenberg mengemukakan bahwa metode eksperimen yang digunakan untuk menemukan posisi atau momentum suatu partikel seperti elektron dapat menyebabkan perubahan, baik pada posisi, momentum atau keduanya.
Teori Schrodinger dan prinsip ketidakpastian Heisenberg melahirkan model atom mekanika kuantum sebagai berikut:
1. Posisi elektron dalam atom tidak dapat ditentukan dengan pasti.
2. Atom mempunyai kulit elektron.
3. Setiap kulit elektron memiliki subkulit elektron.
4. Setiap subkulit elektron memiliki sub-sub kulit elektron.
Kesimpulan Mengenai Model Atom Mekanika Kuantum
Model atom mekanika kuantum didasarkan pada:
1. elektron bersifat gelombang dan partikel, oleh Louis de Broglie (1923).
2. persamaan gelombang elektron dalam atom, oleh Erwin Schrodinger (1926).
3. asas ketidakpastian, oleh Werner Heisenberg (1927).
Menurut teori atom mekanika kuantum, elektron tidak bergerak pada lintasan tertentu. Berdasarkan hal tersebut maka model atom mekanika kuantum adalah sebagai berikut:
a) Atom terdiri atas inti atom yang mengandung proton dan neutron, dan elektronelektron mengelilingi inti atom berada pada orbital-orbital tertentu yang membentuk kulit atom, hal ini disebut dengan konsep orbital.
b) Dengan memadukan asas ketidakpastian dari Werner Heisenberg dan mekanika gelombang dari Louis de Broglie, Erwin Schrodinger merumuskan konsep orbital sebagai suatu ruang tempat peluang elektron dapat ditemukan.
c) Kedudukan elektron pada orbital-orbitalnya dinyatakan dengan bilangan kuantum.
Kelebihan dan Kekurangan Model Atom Mekanika Kuantum
Teori dan model atom mekanika kuantum yang diajukan oleh Erwin Schrodinger berhasil menyempurnakan beberapa kelemahan yang ada dalam teori atom Niels Bohr sekaligus membuka pemahaman baru mengenai struktur atom dan pergerakan elektron di dalam atom.
Berikut ini beberapa keunggulan atau kelebihan teori atom mekanika kuantum (modern):
1. Dapat menjelaskan posisi kebolehjadian ditemukannya elektron.
2. Dapat menjelaskan posisi elektron saat mengorbit.
3. Dapat mengukur perpindahan energi eksitasi dan emisinya.
4. Mengidentifikasi proton dan neutron pada inti sedangkan elektron pada orbitalnya.
Teori atom mekanika kuantum didukung dengan rumusan persamaan gelombang yang ditemukan oleh Schrodinger, yaitu persamaan berupa fungsi suatu ruang tiga dimensi (3D). Kelemahannya, yaitu sebagai berikut.
1. Rumusan persamaan gelombang hanya dapat diterapkan secara eksak untuk partikel dalam kotak dan atom dengan elektron tunggal.
2. Model atom mekanika kuantum sulit diterapkan untuk sistem makroskopis (skala lebih besar) dengan kumpulan atom misalnya pada tumbuhan, hewan dan manusia.
Gallery Model Atom Mekanika Kuantum
 Model Atom Mekanika Kuantum Pdf Free Download
Model Atom Mekanika Kuantum Pdf Free Download
 Teori Atom Mekanika Kuantum Tutorialpelajaran Com
Teori Atom Mekanika Kuantum Tutorialpelajaran Com
 Penjelasan Tentang Teori Atom Mekanika Kuantum Ilmu Sains
Penjelasan Tentang Teori Atom Mekanika Kuantum Ilmu Sains
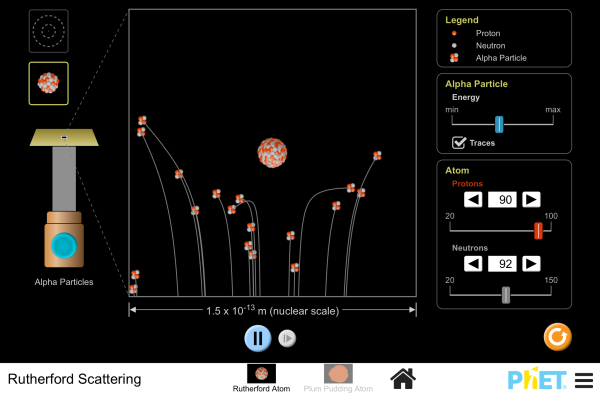
 Hamburan Rutherford Inti Atom Struktur Atom Mekanika
Hamburan Rutherford Inti Atom Struktur Atom Mekanika
 Model Atom Mekanika Kuantum Seputarilmu Com
Model Atom Mekanika Kuantum Seputarilmu Com
 Mekanika Kuantum Kumpulan Stadi Kimia
Mekanika Kuantum Kumpulan Stadi Kimia
 Teori Atom Modern Theres Light At The End Of Every Tunnel
Teori Atom Modern Theres Light At The End Of Every Tunnel
 Teori Atom Modern Dosenpintar Co Id
Teori Atom Modern Dosenpintar Co Id
 Belajar Teori Atom Mekanika Kuantum Bangku Depan
Belajar Teori Atom Mekanika Kuantum Bangku Depan
 Doc Teori Atom Mekanika Kuantum Francius Tampubolon
Doc Teori Atom Mekanika Kuantum Francius Tampubolon
 Teori Model Atom Mekanika Kuantum Smansa Semarang
Teori Model Atom Mekanika Kuantum Smansa Semarang
 Teori Atom Mekanika Kuantum Dan Ikatan Kimia
Teori Atom Mekanika Kuantum Dan Ikatan Kimia
 Teori Atom Mekanika Kuantum Dan Sistem Periodik Mafiadoc Com
Teori Atom Mekanika Kuantum Dan Sistem Periodik Mafiadoc Com
 Model Atom Dalton Thomson Rutherford Bohr Mekanika
Model Atom Dalton Thomson Rutherford Bohr Mekanika
 Pengertian Dan Bunyi Teori Atom Pendidikan
Pengertian Dan Bunyi Teori Atom Pendidikan
 Model Atom Mekanika Kuantum Serta Kelebihan Dan
Model Atom Mekanika Kuantum Serta Kelebihan Dan
 Bilangan Kuantum Bentuk Orbital Atom Contoh Soal
Bilangan Kuantum Bentuk Orbital Atom Contoh Soal
 The Quantum Mechanical Model Of The Atom Article Khan
The Quantum Mechanical Model Of The Atom Article Khan
 B Teori Atom Mekanika Kuantum Nyontek Net
B Teori Atom Mekanika Kuantum Nyontek Net
 Teori Atom Dan Struktur Atom Konfigurasi Elektron Menurut
Teori Atom Dan Struktur Atom Konfigurasi Elektron Menurut
 Perkembangan Model Atom Dari Masa Ke Masa Myrightspot Com
Perkembangan Model Atom Dari Masa Ke Masa Myrightspot Com








0 Response to "Model Atom Mekanika Kuantum"
Post a Comment