Asam Basa Bronsted Lowry
 Pasangan Asam Basa Konjugasi Berdasarkan Teori Asam Basa
Pasangan Asam Basa Konjugasi Berdasarkan Teori Asam Basa
Pengertian Asam dan Basa Menurut Bronsted-Lowry

- Senyawa yang terlibat dalam reaksi harus dalam bentuk larutan.
- Suatu senyawa dikatakan bersifat asam jika dalam larutannya menghasilkan ion H+, sedangkan suatu senyawa dikatakan bersifat basa jika dalam larutannya melepaskan ion OH–.
HCl(g) + NH3(g) ⎯⎯→ NH4Cl(s)
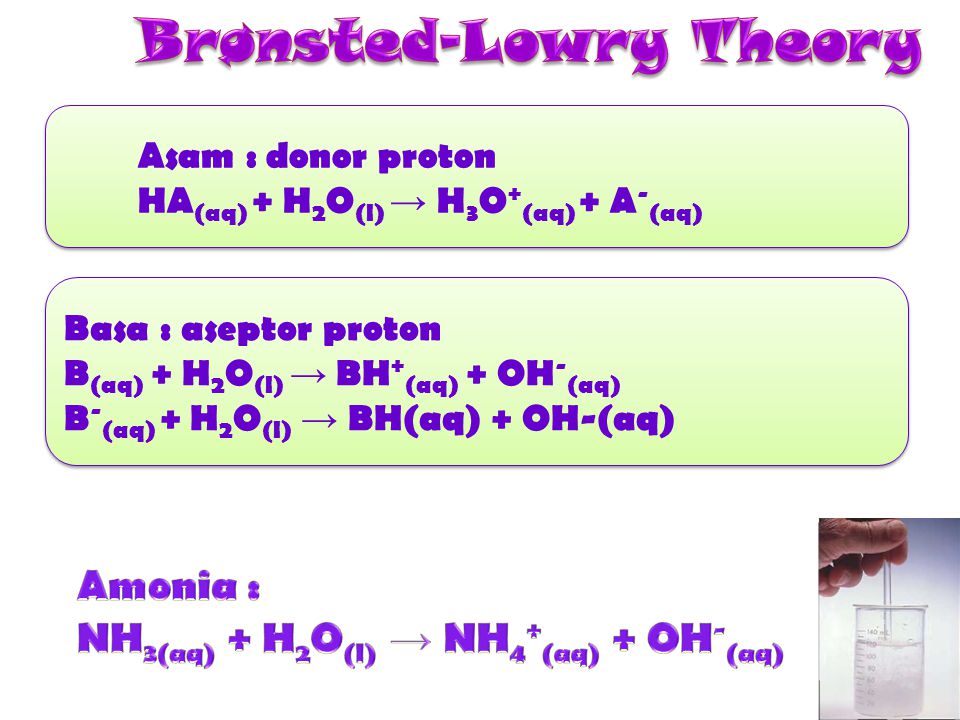
- Asam Bronsted-Lowry = donor proton (H+)
- Basa Bronsted-Lowry = akseptor proton (H+)
- Konsep asam-basa Bronsted-Lowry tidak terbatas dalam pelarut air, tetapi juga menjelaskan reaksi asam-basa dalam pelarut lain atau bahkan reaksi tanpa pelarut.
- Asam-basa Bronsted-Lowry tidak hanya berupa molekul, tetapi juga dapat berupa kation atau anion. Konsep asam-basa Bronsted-Lowry dapat menjelaskan sifat asam dari NH4Cl. Dalam NH4Cl, yang bersifat asam adalah ion NH4+ karena dalam air dapat melepas proton.
Gallery Asam Basa Bronsted Lowry
 Arrhenius Bronsted Lowry Lewis Models Of Acids And Bases
Arrhenius Bronsted Lowry Lewis Models Of Acids And Bases
 Teori Asam Basa Lewis Arrhenius Dan Bronsted Lowry
Teori Asam Basa Lewis Arrhenius Dan Bronsted Lowry
 Teori Asam Basa Industri17imafa
Teori Asam Basa Industri17imafa
 Tentang Kimia Wowkimia Instagram Posts Deskgram
Tentang Kimia Wowkimia Instagram Posts Deskgram
 Kegiatan Belajar 1 Asam Basa A Capaian Pembelajaran
Kegiatan Belajar 1 Asam Basa A Capaian Pembelajaran
 Teori Asam Basa Pengertian Sifat Teori Ahli Dosenpintar Com
Teori Asam Basa Pengertian Sifat Teori Ahli Dosenpintar Com
 Keterbatasan Teori Asam Basa Arrhenius Bronsted Lowry Dan
Keterbatasan Teori Asam Basa Arrhenius Bronsted Lowry Dan
 Teori Asam Basa Bronsted Lowry
Teori Asam Basa Bronsted Lowry
 Teori Asam Basa Asam Basa Arrhenius Asam Basa Bronsted Lowry
Teori Asam Basa Asam Basa Arrhenius Asam Basa Bronsted Lowry
 Chemical Equilibrium For Technological Smk And Agriculture
Chemical Equilibrium For Technological Smk And Agriculture
 Berikan Contoh Yang Dapat Menjelaskan Teori Asam Basa
Berikan Contoh Yang Dapat Menjelaskan Teori Asam Basa
 Acid Base Solutions Acids Bases Equilibrium Phet
Acid Base Solutions Acids Bases Equilibrium Phet
 Bronsted Lowry Asam Basa Teori Dressing Perawatan Luka Penyemprotan Buy Membakar Luka Penyembuhan Dressing Penyemprotan Product On Alibaba Com
Bronsted Lowry Asam Basa Teori Dressing Perawatan Luka Penyemprotan Buy Membakar Luka Penyembuhan Dressing Penyemprotan Product On Alibaba Com
 Teori Asam Basa Bronsted Lowry Dalam Ilmu Kimia
Teori Asam Basa Bronsted Lowry Dalam Ilmu Kimia
 Teori Asam Basa Bronsted Lowry Kelebihan Dan Kelemahan
Teori Asam Basa Bronsted Lowry Kelebihan Dan Kelemahan
 Bab Ii Tinjauan Pustaka Asam Basa Konjugasi Menurut
Bab Ii Tinjauan Pustaka Asam Basa Konjugasi Menurut
 Gambar 3 Reaksi Menurut Asam Basa Bronsted Lowry Download
Gambar 3 Reaksi Menurut Asam Basa Bronsted Lowry Download



0 Response to "Asam Basa Bronsted Lowry"
Post a Comment